在臨床前或臨床試驗中,單細胞表達譜的分子分辨率可用于描述聯合免疫治療中潛在的協同、加性、中性或拮抗的細胞和分子活性。三陰性乳腺癌(TNBC)是一種常對化療產生耐藥性的惡性乳腺癌,這種耐藥性是由于化療對預先存在的克隆的選擇還是化療期間獲得了新的基因突變導致是一個長久未解決的問題。為了探究這個問題,科學家們利用單細胞 RNA-seq、單細胞 DNA-seq 和全外顯子測序研究了 20 名 TNBC 患者在接受新輔助化療(NAC)期間的基因及表達變化,相關研究成果 2018 年發表在《Cell》上 [1]。
深度外顯子測序發現 10 位患者 NAC 導致 clone 消失,而 10 位患者治療后 clone 一直存在,利用單細胞基因組測序探究拷貝數變異,鑒定耐藥基因。對不同治療時期的腫瘤細胞進行差異表達基因分析發現,所有消退型患者在治療后 12 個已知的癌癥基因均下調,部分信號通路也下調。結合分析腫瘤細胞和正常細胞,發現治療后正常細胞亞群中 ACTA2 表達水平高,治療前腫瘤細胞亞群中 EPCAM 表達水平高。探究持續型患者的表型進化,對每個患者進行差異表達分析,僅有少量顯著基因(MYC,ERBB3,KIT,PI3KR1)已知與腫瘤相關,但耐藥基因在治療后出現了高度富集。
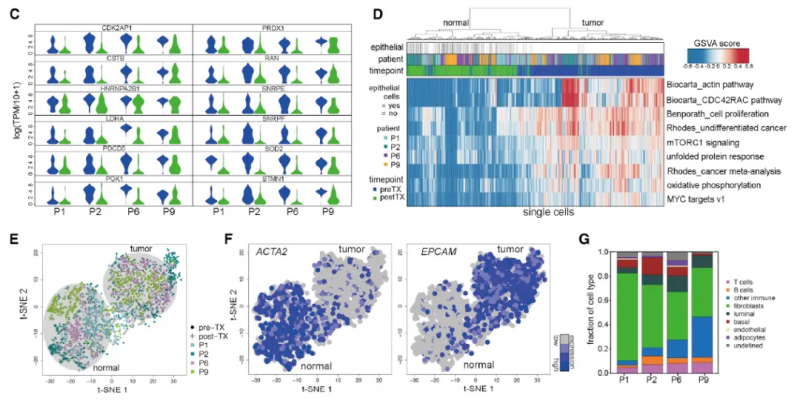
圖 工作流程圖 [1]

圖 CD8 T 細胞細分及功能富集 [1]
參考文獻:
[1]. Kim C, Gao R, Sei E, et al. Chemoresistance Evolution in Triple-Negative Breast Cancer Delineated by Single-Cell Sequencing[J]. Cell, 2018, 173(4):879-893.
更多伯豪生物人工服務:


