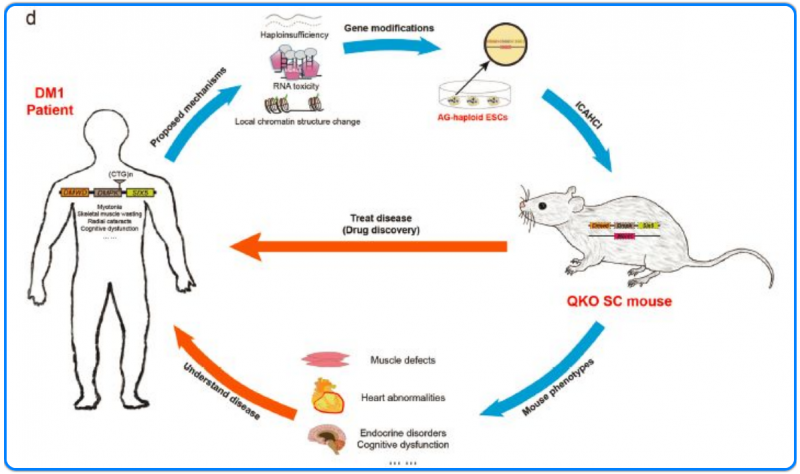
關于強直性肌營養不良 1 型的研究
強直性肌營養不良 1 型(DM1)是一種復雜的遺傳性疾病,主要由肌營養不良肌強直蛋白激酶(DMPK) 基因 3’非編碼區的 CTG 重復擴增引起的。DM1 疾病表型,嚴重程度和發病年齡變異性極高,主要癥狀包括肌強直、肌肉萎縮、肌無力、心臟傳導缺陷、白內障和胰島素抵抗等。2020 年 2 月 5 日,伯豪客戶中科院上海生化細胞所的李勁松及胡蘋研究團隊在 Cell Research 上聯合發表了題為“Dosage effect of multiple genes accounts for multisystem disorder of myotonic dystrophy type 1”的研究論文。研究人員利用半克隆技術將帶有突變 Dmpk、Six5 和 Mbnl1 的單倍體胚胎干細胞注射到小鼠卵母細胞中,建立攜帶多基因雜合突變的小鼠模型來模擬多基因劑量的減少,為開展 DM1 致病機制和藥物篩選研究提供了新模型。

主要研究結果
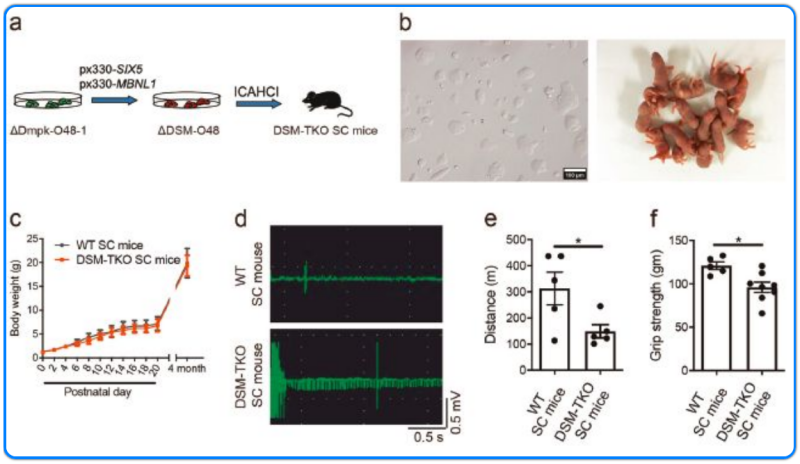
三基因雜合突變模型分析
研究人員首先通過半克隆技術結合 CRISPR/Cas9 基因編輯技術,成功構建了 Dmpk、Six5 和 Mbnl1 雜合突變的孤雄單倍體胚胎干細胞(AG-haESCs),并通過 ICAHCI 技術注入卵子進而一步獲得 Dmpk、Six5 和 Mbnl1 三基因雜合突變的半克隆小鼠模型。全基因組測序分析結果顯示沒有脫靶效應,表型分析顯示該半克隆小鼠產生了肌無力、肌萎縮、嚴重運動障礙、呼吸和消化功能紊亂等典型的 DM1 表型,但沒有先天性 DM1(CDM)的表型,提示其他基因的劑量變化可能與此相關。
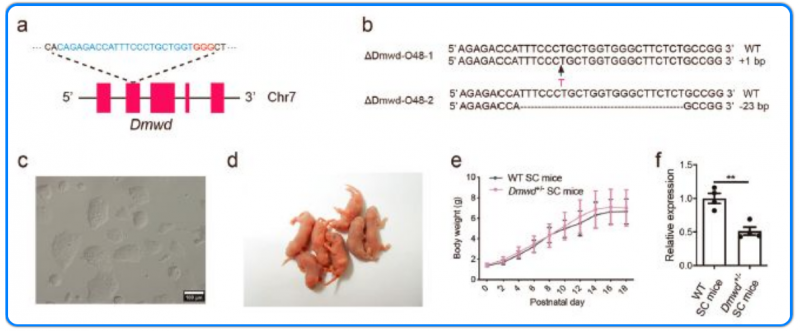
Dmwd 參與 DM1
根據已有研究結果,Dmpk 中 CTG 重復序列的擴增會通過改變局部染色質結構產生等位基因特異性作用,下調 Dmpk 兩個相鄰基因 Six5(Dmpk 的下游)和 Dmwd(Dmpk 的上游)的表達。研究人員通過 CRISPR-Cas9 技術構建 Dmwd 突變細胞并注入小鼠體內,表型分析顯示 Dmwd 突變小鼠肌纖維 CSA 顯著降低,但其他 DM1 表型未被觀察到,提示 Dmwd 突變會影響 DM1 表型,但不足以解釋 DM1 的所有復雜多系統癥狀。
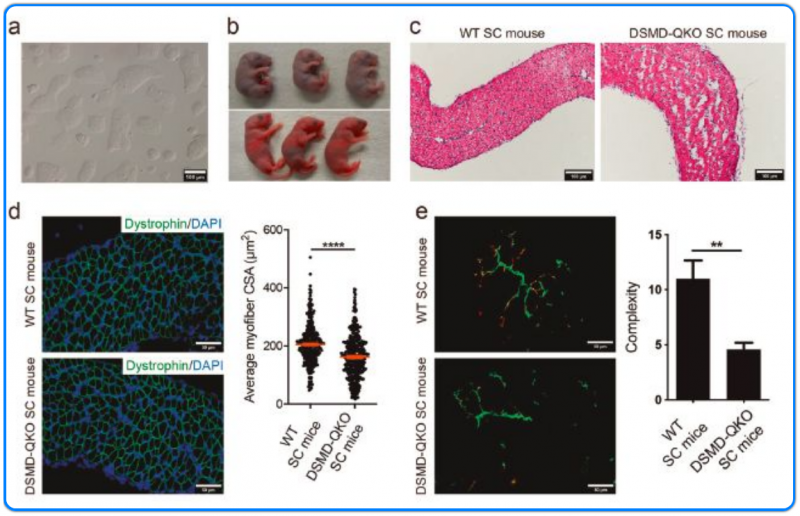
四基因雜合突變模型分析
研究人員進一步構建了 Dmpk、Six5、Mbnl1 和 Dmwd 四基因雜合突變的小鼠模型,以了解更多的 DM1 癥狀。脫靶分析顯示在被測細胞中沒有新的突變位點,表型分析顯示四基因雜合突變小鼠有先天性 DM1 表型,22% 小鼠在出生后數小時內死亡,其主要原因是膈肌發育異常導致的肺擴張失敗。存活小鼠有嚴重的肌強直、肌無力、肌肉萎縮和運動缺陷等一系列典型的 DM1 表型。上述結果表明 Dmwd 參與其中的多基因劑量減少是 DM1 表型產生的主要原因。
MuSCs 分析
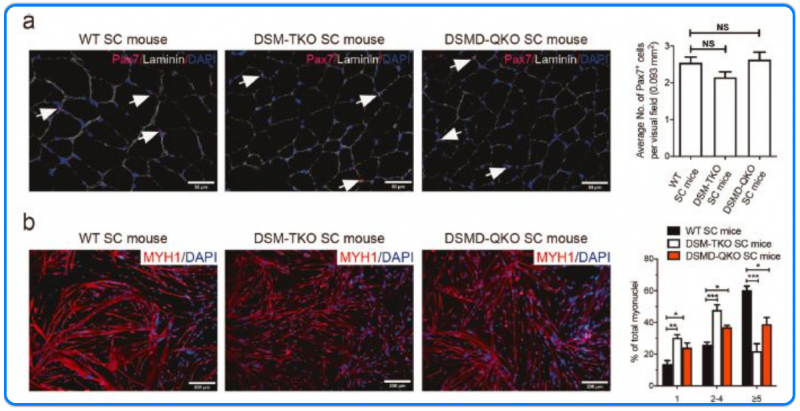
基于已有研究結果顯示 DM1 患者的肌肉干細胞存在缺陷,研究人員對三基因雜合突變和四基因雜合突變小鼠的肌肉干細胞進行了相應的分析,結果顯示,兩種小鼠的肌肉干細胞數量和增殖能力與正常小鼠相比沒有明顯差異,但是肌肉干細胞的干性顯著降低,從而導致肌肉分化的缺陷。全基因組轉錄分析及可變剪切分析(伯豪生物提供)提示干細胞階段分化基因的過早表達導致干細胞特性部分喪失,可能是突變體 MuSCs 體內外分化潛能降低的原因。研究人員進一步建立了促進肌肉干細胞分化的小分子篩選系統,發現 T5381948 在細胞水平上能緩解肌肉分化異常表型,為進一步開展大規模 DM1 藥物篩選研究奠定了基礎。
研究結論
該研究開發了一種新策略,通過半克隆技術快速構建多基因雜合突變小鼠模型來模擬 DM1 的多數表型,一定程度上證明了 Dmpk 中 CTG 重復序列的異常擴增會導致多個基因表達水平下調從而誘發 DM1 的復雜病理表型,這些模型的建立為深入研究 DM1 的發病機理和進行藥物篩選奠定了基礎。